| . |
|
||||||
|
|
| . |
|
||||||
| Les Virus |
|
|
On a d'abord dĂŠsignĂŠ
sous le terme de virus tous les agents infectieux susceptibles de
provoquer l'apparition d'un ensemble morbide quand ils sont introduits
dans un organisme vivant. Le terme s'est ensuite appliquĂŠ Ă tout micro-organisme
infectieux (y compris, par exemple, les bactĂŠries).
Aujourd'hui on n'appelle virus que certaines entitĂŠs microscopiques, dont
la place dans le monde vivant est très singulière, voire problÊmatique.
Bien plus petits et gĂŠnĂŠtiquement plus simples (un seul type d'acide
nuclĂŠique) que les bactĂŠries, les virus n'ont pas de vie indĂŠpendante
de celles des organismes qu'ils parasitent. Ils apparaissent
ainsi comme des entitĂŠs parasitaires non-cellulaires qui ne peuvent ĂŞtre
classÊes dans aucun règne. Ils peuvent infecter des organismes aussi
divers que les archĂŠes, les bactĂŠries procaryotes, les eucaryotes tels
que les champignons, les plantes
et les animaux, et provoquer chez leurs hĂ´tes
de très nombreuses maladies, certaines
mortelles. Il existe mĂŞme des virus de virus, appelĂŠs
virus satellites.
En fait, les virus appartiennent Ă un monde intermĂŠdiaire entre celui
des organismes vivants et celui des entitĂŠs non-vivantes.
Les êtres vivants proprement dits grandissent, mÊtabolisent et se reproduisent. En revanche, les virus, qui ne sont pas cellulaires, n'ont pas de mÊtabolisme; ils ne peuvent pas non plus se dÊvelopper et se reproduire par division cellulaire. Les virus peuvent seulement se copier ou se rÊpliquer. Pour cela, ils dÊpendent entièrement des ressources dÊrivÊes de leurs cellules hôtes pour produire une descendance (des virus sont assemblÊs sous leur forme mature). Les
virus diffèrent beaucoup les uns des autres : leur structure, leurs modes
de rÊplication et les hôtes qu'ils infectent sont très variables. Comment
expliquer cette diversitĂŠ? Alors que la plupart de la diversitĂŠ biologique
peut ĂŞtre comprise Ă travers l'histoire de l'ĂŠvolution (comment les
espèces se sont adaptÊes aux conditions environnementales changeantes
et comment les diffÊrentes espèces sont liÊes les unes aux autres par
une descendance commune), les origines et l'ĂŠvolution des virus
reste inconnue. Les virus n'ont pas laissĂŠ de trace fossile,
aussi personne ne sait exactement quand ni comment les virus ont ĂŠvoluĂŠ
et Ă partir de quelle source ancestrale. Certains virologues soutiennent
que les virus actuels sont une mosaĂŻque d'acides nuclĂŠiques extraits
de diverses sources le long de leurs chemins ĂŠvolutifs respectifs.
CrÊdit : F. A. Murphy / Ecole de mÊdecine vÊtÊrinaire de l'universitÊ de Californie, Davis. DÊcouverte et dÊtection des virus. Si la notion de la contagion des maladies a ÊtÊ entrevue de tout temps, la cause même est restÊe longtemps ignorÊe. Dans le Dictionnaire de LittrÊ  De même qu'il n'y a pas de chaleur sÊparable des corps, mais des variations de tempÊrature, des Êtats chauds et froids de la matière relativement, de même, il n'y a pas de virus en tant qu'espèce de corps ou principes pondÊrables ou isolables. Les virus, pas plus que les miasmes, ne sont non plus des ÊlÊments figurÊs, comme le supposent encore quelques mÊdecins ou micrographes; ce sont des Êtats virulents (totius substantiae) des corps organisÊs  (Dict. LittrÊ et Robin, Êdit. 1878).Grâce aux travaux de Pasteur Le pas dÊcisif a ÊtÊ accompli avec le dÊveloppement d'un filtre en porcelaine - le filtre Chamberland-Pasteur - qui pouvait Êliminer toutes les bactÊries visibles au microscope de tout Êchantillon liquide. En 1886, Adolph Meyer a dÊmontrÊ qu'une maladie des plants de tabac (maladie de la mosaïque du tabac) pouvait être transfÊrÊe d'une plante malade à une plante saine via des extraits de plantes liquides. En 1892, Dmitri Ivanowski a montrÊ que cette maladie pouvait être transmise de cette manière même après que le filtre Chamberland-Pasteur ait retirÊ toutes les bactÊries viables de l'extrait. Il a fallu encore de nombreuses annÊes avant qu'il ne soit prouvÊ que ces agents infectieux  filtrables  n'Êtaient pas simplement de très petites bactÊries et constituaient un nouveau type de minuscules particules pathogènes. A partir de là , on a rÊservÊ le nom de virus aux agents infectieux non bactÊriens. L'Êtape dÊcisive, qui permettra à la virologie de prendre vÊritablement son essor, est franchie en 1949, quand John Enders, Thomas Weller et Frederick Robbins parviennent pour la première fois à cultiver in vitro un virus (celui de la polio). Les aspects physiques et chimiques des virus peuvent dÊsormais être ÊtudiÊs en dÊtail grâce à la disponibilitÊ des grandes quantitÊs de virus ainsi produits. En 1954, AndrÊ Lwoff (auteur en 1964 d'une classification des virus) donne la dÊfinition du virion ( = particule virale responsables de l'infection de cellule à cellule) qui est aujourd'hui encore en vigueur : le virion possède un seul acide nuclÊique à partir duquel il se reproduit; il ne peut ni croÎtre ni se diviser; il ne possède aucune information concernant les enzymes du mÊtabolisme producteur d'Ênergie; la multiplication des virions implique l'utilisation des ressources fournies par la cellule hôte (par leurs ribosomes notamment). Le virion est donc un parasite absolu. On a distinguÊ plus tard les virus de deux autres agents infectieux rÊpondant (entièrement pour le premier et partiellement pour le second) à cette dÊfinition : les viroïdes (ARN non-codant), qui peuvent encore être rangÊs parmi les virus, et les prions (protÊines), qui sont les premiers agents pathogènes connus ne reposant pas sur des gènes formÊs d'un acide nuclÊique. La dÊcouverte des viroïdes date du dÊbut des annÊes 1970 (Theodor Otto Diener). Les prions dont le rôle d'agent infectieux est parfois encore contestÊ aujourd'hui ont ÊtÊ dÊcouverts vers 1980 (Stanley Prusiner). Un
virus c'est tout petit.
à l'exception des grands virions, comme le virus de la variole et d'autres grands virus à ADN, les virus ne peuvent pas être vus au microscope optique. Ce n'est que lors du dÊveloppement du microscope Êlectronique à la fin des annÊes 1930 que les scientifiques ont eu leur premier bon aperçu de la structure du virus de la mosaïque du tabac et d'autres virus. La structure de surface
des virions peut ĂŞtre observĂŠe Ă la fois par microscopie ĂŠlectronique
Ă balayage et Ă transmission, tandis que les structures internes du virus
ne peuvent ĂŞtre observĂŠes que sur les images d'un microscope ĂŠlectronique
Ă transmission. L'utilisation de la microscopie ĂŠlectronique et d'autres
technologies a permis la dĂŠcouverte de nombreux virus de tous les types
d'organismes vivants.
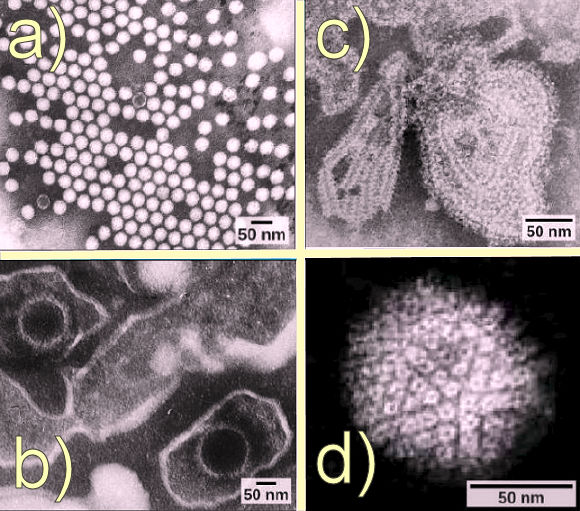
Ăvolution virale, morphologie et classificationEvolution des virus.Bien que les biologistes possèdent une quantitĂŠ importante de connaissances sur la façon dont les virus actuels subissent des mutations et s'adaptent, on en sait beaucoup moins, on l'a dit, sur l'origine des virus. Lorsqu'ils explorent l'histoire ĂŠvolutive de la plupart des organismes, les scientifiques peuvent examiner les archives fossiles et les preuves historiques similaires. Cependant, Ă notre connaissance, les virus ne se fossilisent pas. Les virologues doivent donc extrapoler Ă partir d'enquĂŞtes sur l'ĂŠvolution des virus d'aujourd'hui et en utilisant des informations biochimiques et gĂŠnĂŠtiques pour crĂŠer des histoires spĂŠculatives des virus. La plupart des chercheurs conviennent que les virus n'ont pas un seul ancĂŞtre commun, et qu'il n'y a pas une seule hypothèse raisonnable sur les origines des virus. Il existe actuellement plusieurs scĂŠnarios ĂŠvolutifs qui peuvent expliquer l'origine des virus. ⢠L'une de ces hypothèses, la ÂŤ dĂŠvolution Âť ou hypothèse rĂŠgressive, suggère que les virus ont ĂŠvoluĂŠ Ă partir de cellules indĂŠpendantes ou de parasites procaryotes intracellulaires. Cependant, de nombreuses composantes de la façon dont ce processus aurait pu se produire restent inconnues.Dans tous les cas, les virus continuent probablement d'ĂŠvoluer avec les cellules qu'ils utilisent comme hĂ´tes. Ă mesure que la technologie progresse, les scientifiques pourraient dĂŠvelopper et affiner des hypothèses supplĂŠmentaires pour expliquer les origines des virus. Un domaine ĂŠmergent, appelĂŠ systĂŠmatique molĂŠculaire des virus, s'est donnĂŠ cet objectif en comparant le matĂŠriel gĂŠnĂŠtique sĂŠquencĂŠ. Les chercheurs de cette branche espèrent mieux comprendre l'origine des virus : une dĂŠcouverte qui pourrait conduire Ă des avancĂŠes dans les traitements des maladies dont ces redoutables entitĂŠs sont responsables. Morphologie virale.
Un virion est d'abord constituĂŠ d'un noyau d'acide nuclĂŠique. Celui-ci, souvent ĂŠtroitement associĂŠ Ă des protĂŠines internes, est entourĂŠ d'un revĂŞtement protĂŠique externe rigide, la capside. Ces ĂŠlĂŠments forment ce qu'on appelle la nuclĂŠocapside. La capside peut ĂŞtre nue, mais parfois elle est entourĂŠe d'une enveloppe externe (le pĂŠplos) constituĂŠe de membranes protĂŠiques et phospholipidiques dĂŠrivĂŠes de la cellule hĂ´te. Les virus peuvent ĂŠgalement contenir des protĂŠines supplĂŠmentaires, telles que des enzymes, Ă l'intĂŠrieur de la capside ou attachĂŠes au gĂŠnome viral. La diffĂŠrence la
plus ĂŠvidente entre les membres de diffĂŠrentes familles virales est la
grande diversitĂŠ de leur morphologie. Une caractĂŠristique intĂŠressante
de la complexitĂŠ virale est que la complexitĂŠ de l'hĂ´te n'est pas nĂŠcessairement
en corrĂŠlation avec la complexitĂŠ du virion. Ainsi, certaines des structures
de virions les plus complexes se trouvent-elles dans les bactĂŠriophages,
les virus qui infectent les bactĂŠries, c'est-Ă dire
les organismes vivants les plus simples.
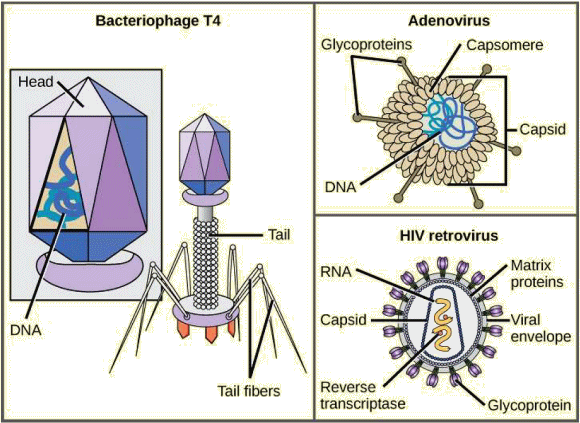
Les
capsides.
En gÊnÊral, les capsides des virus peuvent donc être rangÊes dans trois classes : hÊlicoïdales, icosaÊdriques et complexes. ⢠Les capsides dites à symÊtrie hÊlicoïdale sont longues et cylindriques. De nombreux virus des vÊgÊtaux sont hÊlicoïdaux, par exemple le virus de la mosaïque du tabac.De nombreux virus utilisent un certain type de glycoprotÊine (= protÊine associÊe à un glucide) pour se fixer à leurs cellules hôtes via des molÊcules prÊsentes sur la cellule appelÊes rÊcepteurs viraux. Pour ces virus, la fixation est nÊcessaire afin de permettre une pÊnÊtration ultÊrieure dans la membrane cellulaire; ce n'est qu'après la pÊnÊtration que le virus peut achever sa rÊplication à l'intÊrieur de la cellule. Les rÊcepteurs utilisÊs par les virus sont des molÊcules qui se trouvent normalement à la surface des cellules et qui ont leurs propres fonctions physiologiques. Il semble que les virus aient simplement ÊvoluÊ pour utiliser ces molÊcules pour leur propre rÊplication. Ainsi, le VIH utilise-t-il la molÊcule CD4 des lymphocytes T (globules blancs) comme l'un de ses rÊcepteurs. CD4 est un type de molÊcule appelÊ molÊcule d'adhÊsion cellulaire, qui agit pour maintenir diffÊrents types de cellules immunitaires à proximitÊ les unes des autres lors de la gÊnÊration d'une rÊponse immunitaire des lymphocytes T. Les
enveloppes (pĂŠplos).
L'enveloppe se forme
au moment de la traversĂŠe de la membrane cellulaire, lorsque le virus
nouvellement assemblĂŠ quitte la cellule hĂ´te. Cette enveloppe comprend
des ĂŠlĂŠments d'origine virale et d'autres qui sont pris Ă la cellule.
Elle est constituĂŠe, comme la capside, d'un assemblage d'unitĂŠs de structures,
appelÊes ici plÊplomères. Les propriÊtÊs antigÊniques de surface
de l'enveloppe dĂŠterminent la reconnaissance des cellules sensibles Ă
l'infection et jouent aussi un rĂ´le dans la maturation et la libĂŠration
du virus.
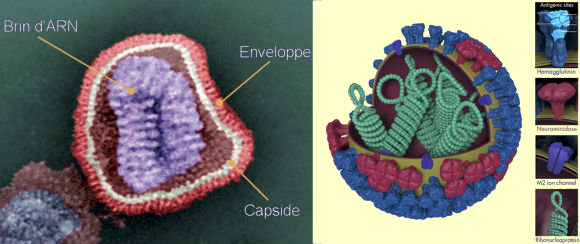
La prÊsence de lipides dans l'enveloppe rend les virus enveloppÊs particulièrement sensibles aux solvants organiques (l'Êther, par exemple). De façon gÊnÊrale, en raison de la fragilitÊ de l'enveloppe, les virus enveloppÊs rÊsistent plus mal que les virus non-enveloppÊs aux changements de tempÊrature, de pH et à certains dÊsinfectants. Parmi les virus
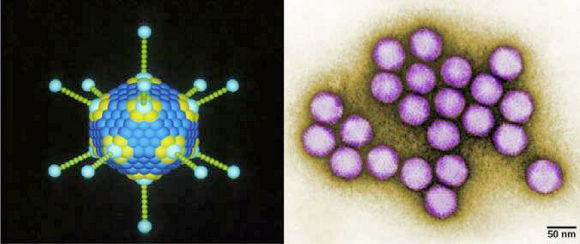
non-enveloppĂŠs ( = Ă nuclĂŠocapside nue), on peut citer ceux qui causent
la polio (Poliovirus), les verrues plantaires (Papillomavirus) et l'hĂŠpatite
A ( Hepatovirus), le virus de la mosaĂŻque du tabac (Tomabovirus),
ou encore l'AdĂŠnovirus (image ci-dessous).
Types
d'acide nuclĂŠique.
Alors que la plupart des virus contiennent un seul acide nuclÊique, d'autres ont des gÊnomes divisÊs en plusieurs segments (fragments subgÊnomiques). Le gÊnome portÊ par l'ARN du virus de la grippe (Myxovirus influenza), par exemple, est dans ce cas (normalement 9 segments). Cette segmentation contribue à sa variabilitÊ et à son Êvolution continue, et explique pourquoi il est difficile de dÊvelopper un vaccin contre la grippe. ⢠Les virus à ADN ne contiennent, comme matÊriel gÊnÊtique, que de l'acide dÊxyribonuclÊique. Celui-ci est gÊnÊralement bicatÊnaire (à double brin), similaire en cela à la double hÊlice dÊcrite par Watson et Crick. Il est rarement circulaire (cas des Papovirus) et donc la plupart du temps linÊaire. Une circularisation de la molÊcule initialement linÊaire peut cependant avoir lieu après l'infection : ce changement de morphologie s'avÊrant nÊcessaire ici pour que l'ADN viral s'intègre dans le chromosome cellulaire.- 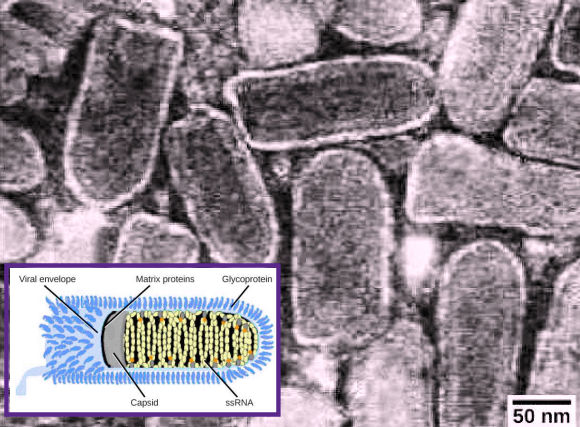
Virus de la rage (Lyssavirus). - C'est un virus enveloppĂŠ, Ă ARN monocatĂŠnaire et Ă capside hĂŠlicoĂŻdale. Comment sont classĂŠs
les virus.
Les biologistes ont cependant proposÊ plusieurs systèmes de classification. Les virus ont ÊtÊ initialement regroupÊs selon leur morphologie. Plus tard, les groupes de virus ont ÊtÊ classÊs selon le type d'acide nuclÊique qu'ils contenaient, ADN ou ARN, et selon que leur acide nuclÊique Êtait simple ou double. La mÊthode de classification la plus couramment utilisÊe aujourd'hui est appelÊe le système de classification de Baltimore, du nom du biologiste David Baltimore, qui l'a dÊveloppÊ au dÊbut des annÊes 1970. Celui-ci est basÊe sur la façon dont l'ARN messager (ARNm) est gÊnÊrÊ dans chaque type particulier de virus. Les
anciens systèmes de classification.
La
classification de Baltimore.
Infections virales et hôtesLes virus sont des parasites intracellulaires obligatoires.Un virus doit d'abord reconnaÎtre et s'attacher à une cellule vivante spÊcifique avant d'y pÊnÊtrer. Après pÊnÊtration, le virus envahisseur doit copier son gÊnome et fabriquer ses propres protÊines. Enfin, les virions descendants doivent s'Êchapper de la cellule hôte pour pouvoir infecter d'autres cellules. Bien que l'on connaisse des virus capables d'infecter en même temps des organismes appartenant à plusieurs phylums, voire à plusieurs règnes, le plus souvent, les virus ne peuvent infecter que certaines espèces d'hôtes et uniquement certaines cellules de cet hôte. Le virus de l'hÊpatite B n'infecte que les Humains, tandis que celui de la poliomyÊlite peut infecter tous les Primates. Tel virus peut aussi infecter plusieurs espèces, en provoquant des maladies très diffÊrentes dans l'une au l'autre espèce ou bien peut provoquer chez l'une une maladie sÊrieuse, tout en ne causant chez une autre aucune maladie. De même, un virus donnÊ, au sein d'une espèce particulière peut être à l'origine de la mort de certains individus, alors que d'autres individus infectÊs ne manifestent aucun symptôme. Les cellules hôtes
spĂŠcifiques qu'un virus doit occuper et utiliser pour se rĂŠpliquer sont
dites permissives. Dans la plupart des cas, la base molĂŠculaire
de cette spÊcificitÊ est dÝe à une molÊcule particulière à la surface
de la cellule hĂ´te et connue sous le nom de rĂŠcepteur viral. Un
rĂŠcepteur viral spĂŠcifique est nĂŠcessaire pour que le virus se fixe.
Les diffĂŠrences de mĂŠtabolisme et de rĂŠponses immunitaires des cellules
hĂ´tes sont aussi un facteur probable intervenant dans la dĂŠtermination
des cellules qu'un virus peut cibler pour sa rĂŠplication.
Ătapes des infections
virales.
Ces changements, appelÊs effets cytopathiques, peuvent modifier les fonctions cellulaires ou même dÊtruire la cellule. Certaines cellules infectÊes, telles que celles infectÊes par le virus du rhume commun (Rhinovirus), meurent par lyse ( = Êclatement) ou apoptose ( = mort cellulaire programmÊe ou -suicide cellulaire-). Cette mort libère en une seule fois tous les virions engendrÊs. Les symptômes des maladies virales rÊsultent à la fois de ces dommages cellulaires causÊs par le virus et de la rÊponse immunitaire au virus, c'est-à -dire de la rÊaction de l'organisme qui tente de contrôler et d'Êliminer le virus. De nombreux virus animaux, tels que le VIH (virus de l'immunodÊficence humaine ou sida), quittent les cellules infectÊes du système immunitaire par un processus appelÊ bourgeonnement, dans lequel les virions quittent la cellule individuellement. Pendant le processus de bourgeonnement, la cellule ne subit pas de lyse et n'est pas immÊdiatement tuÊe. Les dommages que cause le virus aux cellules qu'il infecte peuvent empêcher le fonctionnement normal de celle-ci, même si elles restent en vie pendant un certain temps. Le cycle de rÊplication
des virus, lors d'une infection virale, suit la plupart du temps
des ĂŠtapes similaires : fixation, pĂŠnĂŠtration, rĂŠplication, assemblage
et libĂŠration.
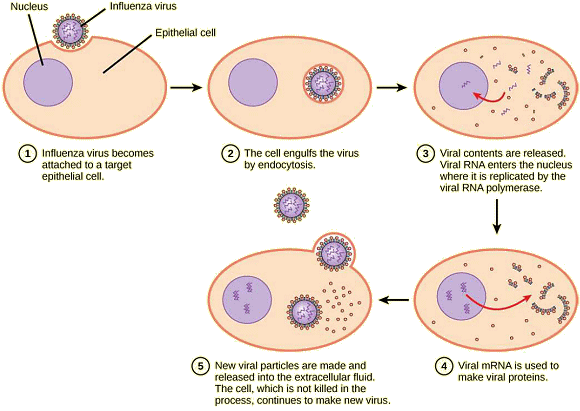
Fixation.
PĂŠnĂŠtration.
⢠Certains virus peuvent pÊnÊtrer dans une cellule hôte sans leur capside : l'acide nuclÊique des bactÊriophages pÊnètre ainsi dans la cellule hôte en laissant la capside à l'extÊrieur de la cellule.Une fois à l'intÊrieur de la cellule, la capside virale se dÊgrade, puis l'acide nuclÊique viral est libÊrÊ et devient disponible pour la rÊplication et la transcription. RÊplication
et assemblage.
⢠Les virus à ADN utilisent gÊnÊralement des protÊines et des enzymes des cellules hôtes pour rÊpliquer l'ADN viral et transcrire l'ARNm viral, qui est ensuite utilisÊ pour piloter à la synthèse des protÊines virales.Ce schÊma connaÎt des exceptions. Si une cellule hôte ne fournit pas les enzymes nÊcessaires à la rÊplication virale, les gènes viraux doivent fournir les informations nÊcessaires pour permettre la synthèse des protÊines manquantes. Les rÊtrovirus, tels que le VIH (groupe VI du système de classification de Baltimore), ont un gÊnome d'ARN qui doit être transcrit en ADN de manière inverse, avant d'être incorporÊ dans le gÊnome de la cellule hôte. Pour convertir l'ARN en ADN, les rÊtrovirus doivent contenir des gènes codants pour l'enzyme transcriptase inverse spÊcifique au virus qui transcrit une matrice d'ARN en ADN. La transcription inverse ne se produit jamais dans les cellules hôtes non infectÊes - l'enzyme transcriptase inverse est uniquement dÊrivÊe de l'expression de gènes viraux dans les cellules hôtes infectÊes. LibÊration. La dernière Êtape de la rÊplication virale est la libÊration des nouveaux virions produits dans l'organisme hôte; ils deviennent alors capables d'infecter les cellules adjacentes et de rÊpÊter le cycle de rÊplication. Comme on l'a vu, certains virus sont libÊrÊs lorsque la cellule hôte meurt et d'autres virus peuvent quitter les cellules infectÊes en bourgeonnant à travers la membrane sans tuer directement la cellule. DiffÊrents hôtes
et leurs virus.
Voyons maintenant les caractĂŠristiques de l'infection virale des cellules procaryotes (bactĂŠries) et eucaryotes (plantes et animaux). BactĂŠriophages.
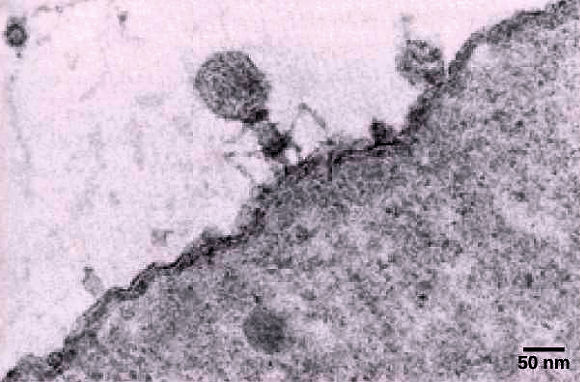
BactĂŠriophage T fixĂŠ sur une bactĂŠrie Escherichia coli. A partir du moment oĂš l'infection d'une cellule par un bactĂŠriophage entraĂŽne la production de nouveaux virions, l'infection est dite productive. Deux situations peuvent alors s'observer. ⢠Le gĂŠnome viral utilise les ressources de la cellule hĂ´te pour se multiplier. Chaque nouvel acide nuclĂŠique viral ainsi produit s'entoure d'une capsule protĂŠique pour former un nouveau virion; la synthèse des protĂŠines ĂŠtant codĂŠe par l'ADN viral, mais la matière première (acides aminĂŠs) et ĂŠnergie (ATP) provenant de la cellule hĂ´te. Les virions, une fois assemblĂŠs, sont libĂŠrĂŠs en faisant ĂŠclater la cellule et peuvent aller infecter d'autres bactĂŠries. On dit dans ce cas que le virus se rĂŠplique via un cycle lytique. Le bactĂŠriophage T4, qui infecte Escherichia coli, fournit un exemple de virus lytique ou virulent. 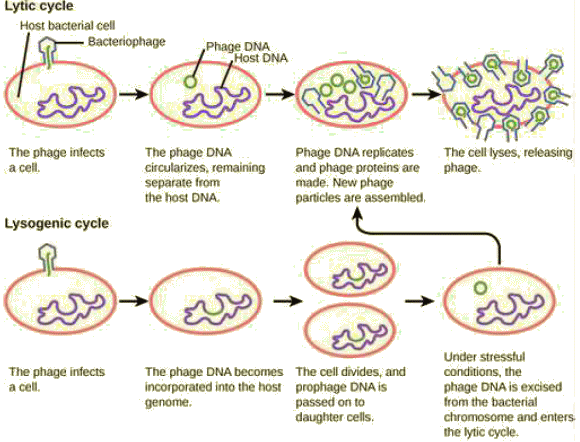
N. B. : Un processus analogue au cycle lysogène s'observe aussi avec le virus des plantes et des animaux. Ces virus peuvent parfois causer des infections oÚ ils ne produisent pas de virions pendant de longues pÊriodes. On parle alors de latence (V. plus pas)..C'est ce qui se produit, par exemple, avec le virus de l'herpès simplex, qui est la cause de l'herpès oral et gÊnital chez l'Humain. Pendant la pÊriode de latence, ce virus peut exister dans le tissu nerveux durant de longues durÊes sans produire de nouveaux virions, puis quitter pÊriodiquement la latence pour provoquer des lÊsions de la peau, qui correspondent à la phase de rÊplication du virus. Les
virus des plantes.
La plupart des virus vĂŠgĂŠtaux, Ă l'instar du virus de la mosaĂŻque du tabac, ont des gĂŠnomes d'ARN monocatĂŠnaire et Ă polaritĂŠ positive (groupe IV de la classification de Baltimore). Cependant, il existe ĂŠgalement des virus vĂŠgĂŠtaux dans la plupart des autres catĂŠgories de virus. Les virus des vĂŠgĂŠtaux
peuvent ĂŞtre transmis d'une plante Ă l'autre par divers vecteurs : par
contact avec la sève d'une plante infectÊe, par des organismes vivants
tels que les insectes et les nĂŠmatodes,
et par le pollen. Contrairement aux bactĂŠriophages,
les virus vĂŠgĂŠtaux n'ont pas de mĂŠcanismes actifs pour dĂŠlivrer le
gĂŠnome viral Ă travers la paroi cellulaire protectrice. Aussi, pour qu'un
virus vÊgÊtal pÊnètre dans une nouvelle plante hôte, un certain type
de dommage mĂŠcanique doit se produire. Ces dommages sont souvent causĂŠs
par les intempĂŠries, les insectes, les animaux
herbivores, le feu ou les activitĂŠs humaines comme l'agriculture ou
l'amĂŠnagement paysager.
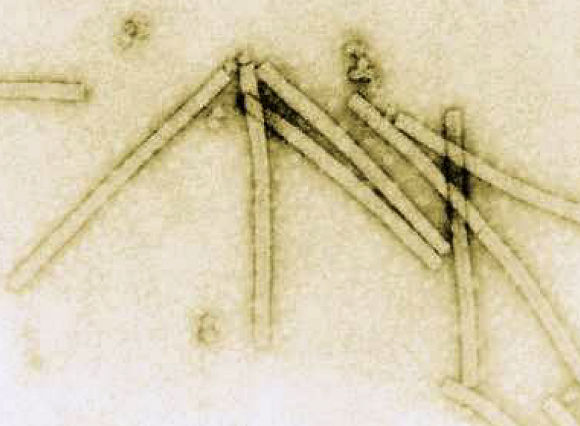
Virus de la mosaïque du tabac (Tobamovirus). Il s'agit d'un virus à capside hÊlicoïdale très allongÊe (longueur 300 nm, diamètre 15 à 20 nm). Il renferme une molÊcule d'ARN composÊe de 6000 nuclÊotides environ. CrÊdit : USDA ARS. Le passage du virus d'une cellule à l'autre au sein d'une plante peut être facilitÊ par la modification virale des plasmodesmes (filaments cytoplasmiques qui passent d'une cellule vÊgÊtale à la suivante). La progÊniture vÊgÊtale peut aussi hÊriter des maladies virales des plantes mères. Le transfert d'un virus d'une plante à une autre est appelÊ transmission horizontale, tandis que l'hÊrÊditÊ d'un virus d'un parent est appelÊe transmission verticale. Les symptômes des
maladies virales varient en fonction du virus et de son hĂ´te. Un symptĂ´me
courant est l'hyperplasie, c'est-Ă -dire la prolifĂŠration anormale
de cellules qui provoque l'apparition de tumeurs vĂŠgĂŠtales appelĂŠes
galles. D'autres virus provoquent une hypoplasie ou une diminution
de la croissance cellulaire dans les feuilles
des plantes, provoquant l'apparition de fines zones jaunes. D'autres virus
encore affectent la plante en tuant directement les cellules vĂŠgĂŠtales
(nĂŠcrose cellulaire). Parmi les autres symptĂ´mes dus Ă l'infection
de virus de vĂŠgĂŠtaux, on peut signaler des feuilles malformĂŠes, des
stries noires sur les tiges des plantes, des altĂŠration de la croissance
des tiges, des feuilles ou des fruits, ou encore
des taches annulaires, qui sont des zones de dĂŠcoloration circulaires
ou linĂŠaires observables sur une feuille.

Feuilles d'orchidĂŠes infectĂŠes par le virus de la mosaĂŻque du tabac. (Image : USDA Forest Service / North Carolina State University). Les virus des plantes peuvent gravement perturber la croissance et le dĂŠveloppement des cultures, affectant considĂŠrablement notre approvisionnement alimentaire. Ils sont responsables parfois de la mauvaise qualitĂŠ et de la faible quantitĂŠ des rĂŠcoltes Ă l'ĂŠchelle mondiale et peuvent entraĂŽner d'ĂŠnormes pertes ĂŠconomiques. Parmi les virus qui infectent les plantes alimentaires, on peut mentionner : le virus de la flĂŠtrissure de la tomate, le virus de la mosaĂŻque commune du haricot et le virus de la mosaĂŻque du concombre. Dans les plantes d'ornement, deux des virus les plus courants sont celui qui occasionne la tache en anneau de la pivoine et le virus de la mosaĂŻque du rosier. Les symptĂ´mes du virus de la mosaĂŻque commune du haricot se traduisent par une baisse de la production de haricots, des rabougrissements et des plants improductifs. Dans le cas de la rose ornementale, la maladie de la mosaĂŻque du rosier provoque des lignes jaunes ondulĂŠes et des taches colorĂŠes sur les feuilles de la plante. Les
virus des animaux.
Les virus des animaux non-enveloppÊs ou nus peuvent pÊnÊtrer dans les cellules de deux manières diffÊrentes : ⢠A partir du moment oÚ une protÊine de la capside virale se lie à son rÊcepteur sur la cellule hôte, le virus peut être introduit à l'intÊrieur de la cellule via une vÊsicule au cours du processus cellulaire normal d'endocytose dont le rÊcepteur est le mÊdiateur. On parle ici d'endocytose mÊdiÊe par les rÊcepteurs.Les virus enveloppÊs ont Êgalement deux façons d'entrer dans les cellules après s'être liÊs à leurs rÊcepteurs : ⢠L'endocytose mÊdiÊe par les rÊcepteurs, similaire à celle que l'on vient de voir pour certains virus non-enveloppÊs. Elle concerne de nombreux virus enveloppÊs, qui pÊnètrent ainsi dans les cellules.Après avoir fabriquÊ leurs protÊines et copiÊ leurs gÊnomes, les virus des animaux achèvent l'assemblage de nouveaux virions et quittent la cellule. Comme nous l'avons dÊjà mentionnÊ à propos du virus de la grippe, les virus animaux enveloppÊs peuvent s'extraire de la membrane cellulaire par bourgeonnement au fur et à mesure qu'ils s'assemblent à partir du matÊriau mis à disposition par la membrane plasmique de la cellule. Il se peut aussi, comme on l'observe avec le rhinovirus, que les descendants viraux non-enveloppÊs s'accumulent dans les cellules infectÊes jusqu'à ce qu'il y ait un signal de lyse ou d'apoptose; dans ce cas, tous les virions sont libÊrÊs ensemble. Comme on va le voir, les virus des animaux sont associÊs à diverses maladies humaines. Certaines d'entre elles (le rhume, la grippe) suivent le schÊma classique de la maladie aiguÍ : les symptômes s'aggravent pendant une courte pÊriode, suivie par l'Êlimination du virus du corps par le système immunitaire, puis par une rÊcupÊration de l'infection. D'autres virus, à l'instar de celui qui cause l'hÊpatite C, provoquent des infections chroniques à long terme, tandis que d'autres encore, comme c'est le cas du virus de l'herpès simplex, ne provoquent que des symptômes intermittents. D'autres virus enfin, peuvent provoquer une maladie chez certains individus et ne donner lieu à aucun symptôme chez d'autres, alors même qu'on est bien en prÊsence d'un infection productive. C'est le cas, dans une proportion encore mal dÊterminÊe, du coronavirus responsable du covid-19 ou encore, plus clairement, des herpèsvirus humains 6 et 7, responsables chez certains patients de la rosÊole, une maladie infantile mineure, et dont l'infection chez d'autres ne donne lieu à aucun symptôme. On dit alors que ces patients ont une infection asymptomatique. Dans les infections
Ă l'hĂŠpatite C, le virus se dĂŠveloppe et se reproduit dans les cellules
hĂŠpatiques, causant des lĂŠsions hĂŠpatiques mineures. Les dommages sont
si faibles que les personnes infectĂŠes ignorent souvent qu'elles sont
infectĂŠes et de nombreuses infections ne sont dĂŠtectĂŠes que par des
analyses de sang de routine sur des patients prĂŠsentant des facteurs de
risque (consommation de drogues par voie intraveineuse).
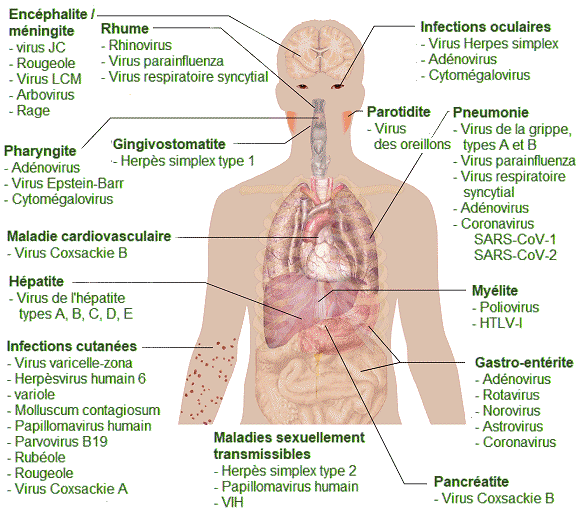
Aperçu
des infections virales chez ls Humains. - Les virus peuvent provoquer
des dizaines
Il convient ici de remarquer que de nombreux symptômes des maladies virales sont causÊs par les rÊponses immunitaires de l'organisme. Il s'ensuit qu'un manque de symptômes signifie alors une faible rÊponse immunitaire au virus. Cela permet au virus d'Êchapper à l'Êlimination par le système immunitaire et de persister chez les individus pendant des annÊes, tout en produisant des virions descendants en faible quantitÊ. On a alors affaire à une maladie virale chronique. Une infection chronique du foie par le virus de l'hÊpatite C augmente les chances de dÊvelopper un cancer du foie, parfois jusqu'à 30 ans après l'infection initiale. Les virus infectant les animaux sur le même mode que le virus de l'hÊpatite C sont appelÊs virus oncogènes, c'est-à -dire qu'ils ont la capacitÊ de provoquer un cancer. Ces virus interfèrent avec la rÊgulation normale du cycle cellulaire hôte soit en introduisant des gènes qui stimulent la croissance cellulaire non rÊgulÊe (oncogènes), soit en interfÊrant avec l'expression des gènes qui inhibent la croissance cellulaire. Les virus oncogènes peuvent être des virus à ADN ou à ARN. Parmi les cancers connus pour être associÊs à des infections virales, on citera le cancer du col de l'utÊrus, causÊ par le papillomavirus humain (HPV) , le cancer du foie causÊ par le virus de l'hÊpatite B, la leucÊmie à cellules T, ainsi que plusieurs types de lymphomes. On l'a vu, le virus de l'herpès simplex peut rester dans un Êtat de latence dans le tissu nerveux pendant des mois, voire des annÊes. Comme le virus -se cache- dans les tissus et produit peu ou pas de protÊines virales, il n'y a rien contre quoi la rÊponse immunitaire puisse agir et l'immunitÊ au virus diminue lentement. Dans certaines conditions (divers types de stress physique et psychologique, par exemple), le virus de l'herpès simplex latent peut être rÊactivÊ et subir un cycle de rÊplication lytique dans la peau, provoquant les lÊsions associÊes à la maladie (apparitions de boutons de fièvre et d'herpès gÊnital). Une fois que les virions sont produits dans les cellules de la peau et que les protÊines virales sont synthÊtisÊes, la rÊponse immunitaire est à nouveau stimulÊe et rÊsout les lÊsions cutanÊes en quelques jours ou semaines en dÊtruisant les virus qui sont dans la peau. Mais, les virus restant dans l'organisme à vie, ce même cycle rÊplicatif, pourra encore se produire par intermittence. Les infections latentes sont Êgalement courantes avec d'autres herpèsvirus, aisni en est-il du virus qui cause la varicelle-zona (herpès humain 3). Dans ce cas, après avoir infectÊ certains individus par la varicelle dans l'enfance, le virus peut rester latent pendant de nombreuses annÊes et se rÊactiver chez l'adulte pour provoquer une affection douloureuse connue sous le nom de zona. PrÊvention et traitement des infections viralesLes maladies causÊes par les virus peuvent être traitÊes par des mÊdicaments antiviraux ou par des vaccins. Il existe cependant des virus, comme le VIH, qui sont capables d'Êviter la rÊponse immunitaire, ce qui les rend rÊtifs aux vaccins, ou encore de muter au sein de l'organisme hôte, ce qui les rend en outre rÊsistants aux mÊdicaments antiviraux.Les vaccins utilisÊs
Ă titre prĂŠventif.
Les vaccins peuvent ĂŞtre prĂŠparĂŠs en utilisant des virus vivants, des virus inactivĂŠs ou des sous-unitĂŠs molĂŠculaires du virus. (Les vaccins viraux inactivĂŠs et les sous-unitĂŠs de virus sont tous deux incapables de provoquer la maladie). La pandĂŠmie de covid-19 a ĂŠtĂŠ l'occasion de mise au point par plusieurs laboratoires d'un tout nouveau type de vaccins Ă destination des humains, les vaccins Ă ARN messager. Les vaccins viraux
vivants sont conçus en laboratoire pour provoquer peu de symptômes chez
les receveurs, tout en leur confĂŠrant une immunitĂŠ protectrice contre
les infections futures. La lutte contre la poliomyĂŠlite a reprĂŠsentĂŠ
une ĂŠtape importante dans l'utilisation des vaccins. Les campagnes massives
de vaccination dans les annĂŠes 1950 (vaccin inactivĂŠ) et 1960 (vaccin
vivant) ont considÊrablement rÊduit l'incidence de la maladie. Ce succès
du vaccin contre la polio a ouvert la voie Ă la dispensation systĂŠmatique
de vaccins infantiles contre la rougeole, les oreillons, la rubĂŠole, la
varicelle et d'autres maladies.
La vaccination a pour but de doper les dÊfenses immunitaires de l'organisme pour que celui-ci soit mieux armÊ pour combattre l'infection virale. Les vaccins vivants sont gÊnÊralement fabriquÊs en attÊnuant (affaiblissant) le virus -de type sauvage- (causant la maladie), en le cultivant en laboratoire dans des tissus ou à des tempÊratures qui diffèrent de ce à quoi le virus est habituÊ chez l'hôte. Les adaptations à ces nouvelles cellules ou tempÊratures induisent des mutations dans les gÊnomes du virus, lui permettant de mieux se dÊvelopper en laboratoire tout en inhibant sa capacitÊ à provoquer des maladies lorsqu'il est rÊintroduit dans des conditions trouvÊes chez l'hôte. Ces virus attÊnuÊs provoquent donc toujours une infection, mais ils ne se dÊveloppent pas très bien, permettant à la rÊponse immunitaire de se dÊvelopper à temps pour prÊvenir une maladie grave. Le problème de l'utilisation de vaccins vivants (qui sont gÊnÊralement plus efficaces que les vaccins inactivÊs) est le risque faible mais significatif que ces virus reviennent à leur forme pathogène par des mutations inverses. Ces mutations se produisent lorsque le vaccin subit des mutations chez l'hôte de telle sorte qu'il se rÊadapte à l'hôte, pouvant à nouveau provoquer une maladie, qui peut ensuite se propager à d'autres humains lors d'une ÊpidÊmie. Ce type de scÊnario s'est produit, par exemple, en 2007 au NigÊria, oÚ des mutations dans un vaccin contre la polio ont conduit à une ÊpidÊmie de cette maladie dans le pays. Les vaccins à ARN messager procèdent
d'une logique diffĂŠrente des autres vaccins. Ordinairement, l'ARN messager
(ARNm) est une molĂŠcule produite dans le noyau d'une cellule,
et qui est porteuse des informations nĂŠcessaires Ă la production d'une
protĂŠine donnĂŠe ( Certains vaccins sont en dĂŠveloppement continu car il existe des virus, tels que la grippe et le VIH, qui ont un taux de mutation ĂŠlevĂŠ par rapport Ă celui d'autres virus et cellules hĂ´tes normales. Dans le cas de la grippe, des mutations qui modifient les molĂŠcules de surface du virus empĂŞchent l'organisme de bĂŠnĂŠficier de l'immunitĂŠ protectrice qui a pu ĂŞtre obtenue lors d'une saison grippale prĂŠcĂŠdente, ce qui oblige les individus Ă se faire vacciner chaque annĂŠe. D'autres virus, tels
que ceux qui causent les maladies infantiles, la rougeole, les oreillons
et la rubĂŠole, mutent si rarement que le mĂŞme vaccin est utilisĂŠ annĂŠe
après annÊe.
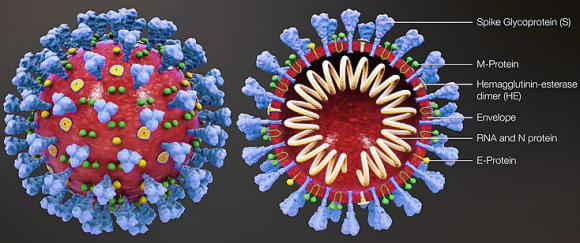
Le SARS-CoV-2, virus du covid-19, une maladie particulièrement contagieuse, identifiÊe à Wuhan en Chine, en novembre 2019, et qui a pris une dimension pandÊmique en moins de 3 mois. Sa gravitÊ parfois, et sa mortalitÊ dans un petit mais non nÊgligeable nombre de cas, ajoutÊes à l'absence de traitement et de vaccin expliquent qu'elle ait eu un impact majeur et sans prÊcÊdent sur l'Êconomie et la vie sociale de toute la planète. modèle 3D : scientificanimations.com. Les vaccins et
les mĂŠdicaments antiviraux utilisĂŠs pour le traitement.
Dans le cas de la rage, une maladie neurologique mortelle transmise par la salive des animaux infectÊs par le virus de la rage, la progression de la maladie depuis le moment de la morsure de l'animal jusqu'à son entrÊe dans le système nerveux central (temps d'incubation) peut durer de deux semaines à six semaines. C'est assez de temps pour vacciner les individus supposÊs avoir ÊtÊ mordus par un animal enragÊ, et permettre une rÊponse immunitaire renforcÊe, suffisante pour empêcher le virus de pÊnÊtrer dans les tissus nerveux. Ainsi, les consÊquences neurologiques potentiellement mortelles de la maladie sont ÊvitÊes. Cette approche a
commencÊ à être mise en oeuvre pour le traitement de la fièvre Êbola,
provoquĂŠe par l'un des virus les plus foudroyants et meurtriers que l'on
connaisse. Transmise par les chauves-souris et les grands singes, cette
maladie peut provoquer la mort de 70 Ă 90% des Humains infectĂŠs en deux
semaines. En utilisant de tout nouveaux vaccins qui renforcent la rĂŠponse
immunitaire de cette manière, on espère que les personnes atteintes seront
mieux Ă mĂŞme de contrĂ´ler le virus, ce qui pourrait sauver d'une mort
rapide et très douloureuse un plus grand pourcentage de personnes infectÊes.

Le virus ebola. - Responsable d'ÊpidÊmies de fièvres hÊmorragiques en Afrique centrale et en Afrique de l'Ouest, c'est un virus linÊaire, à ARN monocatÊnaire, qui contient 19 000 nuclÊides, codant 8 protÊines. (CrÊdits : images en microscopie à balayage, à gauche : Cynthia Goldsmith / CDC; et, à droite, en microscopie à transmission : Thomas W. Geisbert / Ecole de mÊdecine de l'universitÊ de Boston). Les
traitements.
Dans le cas de la plupart des virus, ces mÊdicaments peuvent inhiber le virus en bloquant les actions d'une ou plusieurs de ses protÊines. Il est important de noter que les protÊines ciblÊes doivent être codÊes par des gènes viraux et que ces molÊcules doivent être absentes de la cellule hôte saine. De cette façon, la croissance virale est inhibÊe sans endommager l'hôte. Des antiviraux particuliers ont ÊtÊ dÊveloppÊs pour traiter l'herpès gÊnital (herpès simplex II) et les grippes A et B. ⢠Dans le cas de l'herpès gÊnital, des mÊdicaments tels que l'acyclovir peuvent rÊduire le nombre et la durÊe des Êpisodes de maladie active, au cours desquels les patients dÊveloppent des lÊsions virales dans leurs cellules cutanÊes. Comme le virus reste latent dans les tissus nerveux du corps à vie, ce mÊdicament n'est pas curatif mais peut rendre les symptômes de la maladie plus faciles à gÊrer. 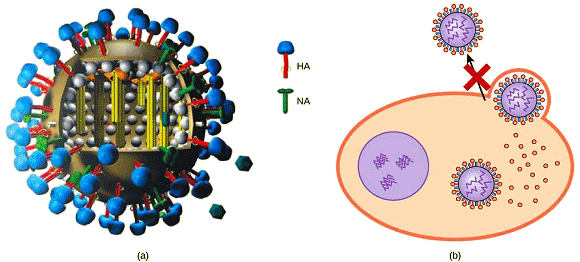
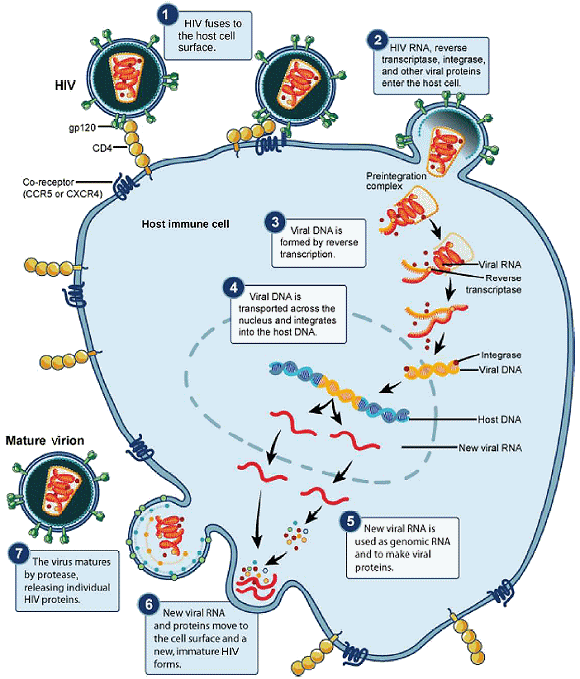
D'autres mÊdicaments antiviraux, tels que la ribavirine, ont ÊtÊ utilisÊs pour traiter diverses infections virales, bien que son mÊcanisme d'action contre certains virus reste incertain. L'application la plus rÊussie - et de loin - d'un traitement basÊ sur des antiviraux concerne le rÊtrovirus VIH, à l'origine d'une maladie qui, si elle n'est pas traitÊe, est gÊnÊralement mortelle dans les 10 à 12 ans après l'infection. Les mÊdicaments anti-VIH peuvent contrôler la rÊplication virale au point que les individus recevant ces mÊdicaments survivent beaucoup plus longtemps que les non traitÊs. Les mÊdicaments anti-VIH inhibent la rÊplication virale à plusieurs Êtapes du cycle de rÊplication du VIH (schÊma ci-dessous) : des mÊdicaments inhibent la fusion de l'enveloppe virale du VIH avec la membrane plasmique de la cellule hôte (inhibiteurs de fusion), d'autres la conversion de son gÊnome ARN en ADN double brin (inhibiteurs de la transcriptase inverse, comme l'AZT), d'autres encore l'intÊgration de la l'ADN viral dans le gÊnome hôte (inhibiteurs d'intÊgrase) et d'autre enfin le traitement des protÊines virales (inhibiteurs de protÊase). Malheureusement,
lorsque l'un de ces mĂŠdicaments est utilisĂŠ individuellement, le taux
de mutation ĂŠlevĂŠ du virus lui permet de dĂŠvelopper facilement et rapidement
une rĂŠsistance au mĂŠdicament, ce qui limite son efficacitĂŠ. La percĂŠe
dans le traitement du VIH a ĂŠtĂŠ le dĂŠveloppement de la multithĂŠrapie
antirĂŠtrovirale HAART, qui implique un mĂŠlange de diffĂŠrents mĂŠdicaments,
parfois appelĂŠs ÂŤ cocktail Âť. En attaquant le virus Ă diffĂŠrents stades
de son cycle rĂŠplicatif, il est beaucoup plus difficile pour le virus
de dĂŠvelopper une rĂŠsistance Ă plusieurs mĂŠdicaments en mĂŞme temps.
Cependant, mĂŞme avec l'utilisation de la thĂŠrapie combinĂŠe HAART, on
craint qu'avec le temps, le virus dĂŠveloppe une rĂŠsistance Ă cette thĂŠrapie.
Ainsi, de nouveaux mĂŠdicaments anti-VIH sont constamment dĂŠveloppĂŠs
dans l'espoir de continuer Ă contrer ce virus hautement mortel.
Autres entitÊs non-cellulaires : viroïdes et prionsViroïdes.Les viroïdes, que l'on divise en deux familles (les PospiviroïdÊs et les AvsunviroïdÊs) sont des agents pathogènes des plantes (on ne connaÎt pas encore de maladie humaine ou animale causÊe par des viroïdes). Il s'agit de petites particules d'ARN circulaires monocatÊnaires qui sont beaucoup plus simples qu'un virus. Les viroïdes n'ont pas de capside ou d'enveloppe extÊrieure, mais de même que les virus, ils sont incapables de se reproduire autrement qu'à l'intÊrieur d'une cellule hôte. Contrairement aux virus, cependant, ils ne fabriquent aucune protÊine et ils ne produisent qu'une seule molÊcule d'ARN spÊcifique. Les viroïdes sont responsables des mauvaises rÊcoltes et de la perte importantes de revenus agricoles chaque annÊe. Les pommes de terre, les concombres, les aubergines, les pêchers, les tomates, les chrysanthèmes, les avocatiers et les cocotiers figurent parmi les plantes qu'ils infectent. Prions.
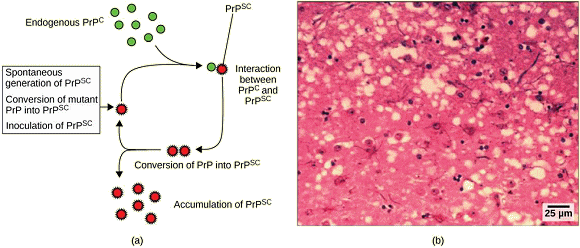
L'idÊe de l'existence d'agents infectieux n'utilisant pas d'acides nuclÊiques a tardÊ à être admise. Il a fallu attendre la fin des annÊes 1970 et les travaux de Stanley Prusiner sur la tremblante du Mouton, puis, au milieu des annÊes 1980, sur la maladie de Creutzfeldt-Jakob et diverses encÊphalopathies spongiformes humaines et animales, pour que de telles entitÊs s'imposent progressivement comme l'objet d'Êtudes. Parmi les maladies neurodÊgÊnÊratives fatales transmises par des prions, on peut mentionner le kuru (très proche de la maladie de Creutzfeldt-Jakob) chez l'Humain et l'encÊphalopathie spongiforme bovine (ESB ou maladie de la vache folle) chez les Bovins, deux maladies dont on a montrÊ qu'elles se sont propagÊes par la consommation de viande, de tissu nerveux ou d'organes internes par des reprÊsentants de la même espèce : consommation de chair humaine par les Humains et consommation de farines animales par les Bovins. ⢠Le kuru, rencontrÊ dans les annÊes 1950 dans l'Est de la Papouasie-Nouvelle-GuinÊe, s'est propagÊ d'Humain à Humain via le cannibalisme rituel.Les individus atteints de kuru et d'ESB prÊsentent des symptômes de perte de contrôle moteur et de comportements inhabituels (par exemple des Êclats de rire incoercibles dans le cas du kuru), suivis de la mort. L'abandon du cannibalisme rituel, d'une part, et le renoncement à l'usage des farines animales pour l'alimentation du bÊtail, d'autre part, ont permis d'endiguer grandement la propagation de ces deux maladies. Les chercheurs ont d'abord cru que encÊphalopathie spongiforme bovine ne touchait que les Bovins. Mais les lÊsions de leur tissu cÊrÊbral se sont avÊrÊes très similaires à celles causÊes par une encÊphalopathie affectant les Humains, et connue sous le nom de variante de la maladie de Creutzfeldt-Jakob (MCJ). Il a pu être montrÊ que cette nouvelle maladie pouvait être acquise en mangeant de la viande provenant d'animaux infectÊs par l'ESB. Cela a conduit divers pays à interdire l'importation de boeuf britannique et causant des dommages Êconomiques considÊrables à la filière dans ce pays. L'ESB existe toujours dans certaines zones gÊographiques. Il s'agit dÊsormais d'une maladie rare, mais toujours difficile à traiter. La maladie peut aussi se propager d'Humain à Humain par le sang, de sorte que de nombreux pays ont interdit le don de sang dans les rÊgions associÊes à l'ESB. La cause des encÊphalopathies spongiformes, telles que le kuru et l'ESB, est une variante structurelle infectieuse d'une protÊine cellulaire normale appelÊe PrP (protÊine prion). C'est cette variante qui constitue la particule nommÊe prion. La PrP existe sous
deux formes, la PrPc, la forme normale
de la protĂŠine, et la PrPsc, la forme
infectieuse. Une fois introduit dans le corps, le PrPsc
contenu dans le prion se lie Ă la PrPc
et la convertit en PrPsc. Cela conduit
Ă une augmentation exponentielle de la protĂŠine PrPsc,
qui s'agrège. La PrPsc est pliÊe anormalement
et la conformation (forme) qui en rĂŠsulte est directement responsable
des lĂŠsions observĂŠes dans le cerveau des bovins infectĂŠs.
(D'après des publications de la collection Openstax
de l'UniversitĂŠ Rice).
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
| . |
|
|
|
|||||||||||||||||||||||||||||||
|